В пищевой промышленности разрешены к применению самые разные добавки, и если обратиться к перечням веществ, допущенных к применению в соответствии с нормативными актами разных стран, то можно увидеть, что их существует весьма немало.
В данной главе речь пойдет только о тех веществах, которые достаточно часто используются в кондитерской промышленности. При принятии решения о возможности применения конкретного вещества технологу всегда следует обращаться к действующим нормативным документам. Сведения по поводу возможной нежелательности использования определенных добавок мгновенно получают огласку в средствах массовой информации, в связи с чем многие фирмы- производители пищевых продуктов стремятся исключить использование любых веществ, которые могли бы быть признаны «добавками». Вместе с тем, отказаться от них оказывается непросто — например, при производстве джемов или желе для усиления вкуса и улучшения желирования может добавляться лимонная кислота. При этом она может быть призана добавкой даже в том случае, когда она является природным компонентом фруктов, используемых для производства джема.
Признаваемое на международном уровне определение пищевых добавок установлено комиссией «Codex Alimentanus», а в Великобритании действуют и «Правила этикетирования пищевых продуктов» (Food Labelling Regulations, 1984). В последнем документе приводится следующее определение: «Пищевая добавка — это любое вещество, которое обычно не считается пищевым продуктом и не употребляется в качестве такового и которое добавляется в пищевые продукты или используется в них (или на их поверхности) на любом этапе производства в целях изменения сроков годности, текстуры, консистенции, внешнего вида, вкуса, запаха, щелочных или кислотных свойств, а также для улучшения перерабатываемое™ пищевых продуктов (включая и вещества для улучшения технологических свойств, добавляемые или используемые вышеуказанным способом)».
Следует отметить, что витамины, нутриенты, соль и некоторые другие вещества к пищевым добавкам не относят.
Кислоты, используемые в кондитерской промышленности
В кондитерские изделия кислоты добавляют в разных целях. Они обеспечивают определенный вкусовой эффект, и поэтому их использование является необходимым при производстве кондитерских изделий с фруктовым вкусом. Кислоты изменяют водородный показатель (pH) продукта, позволяя таким образом контролировать желеобразование пектинового желе. Низкий pH приводит также к некоторой инверсии сахара (сахарозы) во время кипячения, и если этот процесс не регулировать, то могут возникать определенные сложности. Кислотность обладает некоторым консервирующим действием, которое отчасти можно объяснить с точки зрения pH, а отчасти — свойствами самого кислотного радикала. Значительным консервирующим действием обладают уксусная кислота и сорбиновая кислоты.
Первоначально для производства сахарных кондитерских изделий использовалась в основном винная кислота. В настоящее время вместо нее чаще применяют лимонную кислоту.
При непрерывной технологии производства леденцовой карамели кислоты и ароматизаторы добавляют непосредственно в сваренный сироп при его охлаждении. Добавление кристаллической лимонной кислоты приводит к возникновению проблем.
В настоящее время используют забуференную молочную кислоту в жидкой форме, которую легче равномерно смешать с сиропом. На растворы сахара забуфе- ренная молочная кислота оказывает значительно меньшее инвертирующее воздействие, чем лимонная или винная.
Лимонная кислота
Лимонная кислота (СООН СH2С(ОН)СООНСН2 СООН) в природе встречается в лимонном соке, из которого она была впервые выделена в 1784 г. Шиле {Scheele). Вначале кислота, поставляемая для промышленных целей, производилась из лимонного сока, но в настоящее время ее получают с помощью ферментации сахарного сиропа или мелассы под действием определенных плесневых грибов. Эта кислота выпускается как в безводной форме, так и в виде моногидрата; она лишена запаха, бесцветна и легко растворяется в воде (50%-ный раствор) и в спирте (ректифицированном) — 35-40%-ный раствор.
Для производства большинства видов кондитерских изделий ее используют в виде 50%-ного раствора, но для леденцовой карамели может применяться и кислота в порошке. В связи с этим следует учитывать различные температуры плавления кристаллических безводных кислот (у безводной кислоты температура плавления составляет 153°С, а у моногидрата точная температура плавления отсутствует — при нагревании вещество теряет кристаллизационную воду и в конечном счете плавится при температуре около 130°С).
При температуре, когда партию сахарного сиропа выливают на стол, моногидрат плавится, а безводная кислота — нет (при этом моногидрат добавляет к партии небольшое количество влаги). При использовании безводной кислоты для обеспечения хорошей растворимости порошок должен быть очень мелким. При недостаточной дисперсии порошка кислота концентрируется в отдельных частях конфет, вызывая нежелательный резкий вкус.
Состав:
| Моногидрат в виде С6Н807Н20 | 99,5-101,0% |
| Безводная кислота в виде С6Н807 | Не менее 99,0% |
| Остаток при сжигании | Не более 0,05% |
| Сульфаты | Отсутствуют |
| Соль щавелевой кислоты | Отсутствует |
| Тяжелые металлы (свинец, медь, железо) | Не более 10 ppm (частей на миллион) |
| Легко карбонизирующиеся вещества | Только светло-коричневого цвета (по тесту фармакопеи Великобритании) |
Винная кислота
Винная кислота (СООН СН(ОН) СН(ОН) СООН) производится из битартрата калия (виннокислого калия), отделяемого в виде осадка при производстве вина.
В чистом виде это вещество безводно и представляет собой бесцветные кристаллы, температура плавления которых составляет 169 °С. Оно быстро растворяется в воде, и возможно получить 60%-ный раствор. Эта кислота также растворяется в этиловом и изопропиловом спирте. В прошлом ее в больших количествах использовали в кондитерском производстве, но в настоящее время ее вытеснила лимонная кислота.
Вкус винной кислоты резче, чем у лимонной. Были отмечены случаи, когда при использовании винной кислоты в сочетании с некоторыми видами цитрусовых масел возникал неприятный привкус, поэтому при их использовании необходимо применять лимонную кислоту.
Состав:
| Безводная кислота | Не менее 99,7% |
| Потеря при сушке при температуре 105°С | Менее 0,5% |
| Сульфаты | Отсутствуют |
| Соль щавелевой кислоты | Отсутствует |
| Тяжелые металлы (свинец, медь, железо) | Не более 10 ppm |
Фумаровая кислота
Фумаровая кислота (НООС*СН=СН*СООН) является безводным кристаллическим веществом, растворимым в воде лишь в небольшой степени. Она содержится в Fumaria officinalis и различных видах грибов.
Это вещество используется в пищевых продуктах в качестве подкислителя, особенно если требуется не допустить слипания частиц (например в щербетах — порошках для приготовления шипучих напитков). Фумаровая кислота негигроскопична и обладает сильно выраженным приятным кислым вкусом. Применяется она в желатиносодержащих изделиях для повышения прочности желе, а также для повышения взбиваемости яичного альбумина.
Состав:
| Безводная кислота | 99,8% (не менее 99,5%) |
| Содержание влаги | Менее 0,2% |
| Хлориды | Не более 10 ppm |
| Сульфаты | Не более 25 ppm |
| Яблочная кислота | Менее 0,2% |
| Тяжелые металлы (свинец, медь, железо) | Не более 10 ppm |
Эта кислота не плавится — при температуре около 200 °С происходит ее сублимация.
Растворимость в воде:
| При 25 °С | -0,6% |
| 40 °С | — 1,1 % |
| 60 °С | -2,4% |
| 100 °С | -9,8% |
Яблочная кислота
Яблочная кислота (СООН*СН2 СН(ОН) СООН) является естественно встречающейся в природе кислотой, широко распространенной в растительном мире, особенно в незрелых яблоках, а также в винограде, айве и рябине.
Эта кислота образует безводные негигроскопичные бесцветные кристаллы, плавящиеся при 130 °С. Они легко растворимы в воде — почти 60%-ный раствор можно получить при температуре 25 °С.
Яблочная кислота нетоксична и особенно ценится в качестве подкислителя при производстве леденцовой карамели — в этом случае ее зачастую используют в сочетании с молочной кислотой. Эти кислоты могут быть забуферены, в результате чего у них будет достаточно высокий pH, позволяющий снизить уровень инвертирования, сохраняя при этом кислый вкус изделий. Это особенно важно в тех случаях, когда кислоты, ароматизаторы и красители добавляют в высококонцентрированный сироп при непрерывной технологии производства леденцовой карамели. В качестве буфера используют молочнокислый натрий (см. следующий раздел).
Состав и чистота этого вещества сходны с показателями, приведенными для винной и фумаровой кислот.
Молочная кислота
Молочная кислота (СН3СН(ОН)СООН) является естественной природной кислотой, производимой путем ферментации таких сахаров, как лактоза, сахароза и декстроза, а также других близких по свойствам веществ, в том числе из крахмала и различных камедей. Брожение вызывается молочнокислыми бактериями.
Промышленно применяемая молочная кислота представляет собой некристал-лизующуюся густую гигроскопичную жидкость, способную смешиваться с водой и этиловым спиртом. Молочная кислота, используемая в производстве, представляет собой рацемическую смесь оптических изомеров кислоты с небольшим преобладанием правовращающей составляющей. Этот подкислитель обладает приятным вкусом. Кислота может быть забуферена в целях добавления непосредственно в состав карамели — в этом случае кислота препятствует инвертированию. В качестве буферной соли применяют жидкий молочнокислый натрий, удобный для смешивания с молочной кислотой.
Другим важным свойством, характеризующим молочную кислоту, является растворимость молочнокислого кальция. Во многих плодах, камедях и даже в природной воде содержится значительное количество кальция, которое в случае, когда в качестве подкислителя используется лимонная кислота, выпадает в осадок в виде мутной взвеси. При применении молочной кислоты этой проблемы не возникает, что особенно важно при производстве фруктовых жевательных конфет, так как эта продукция должна остаться яркой и прозрачной.
Молочную кислоту можно считать слабым консервантом, хотя она и не обладает общими бактерицидными свойствами.
Эту кислоту используют для предотвращения ферментации в помадных массах с низкой концентрацией жидкой фазы; кислота в концентрации 0,2-0,4% эффективно воздействует на сироп с концентрацией не менее 70%. В этом отношении молочная кислота сходна с уксусной, но обладает значительно менее выраженными вкусовыми свойствами, однако уксусная кислота может эффективно применяться и при значительно более низкой концентрации (см. ниже).
Состав:
| Температура плавления | 16,8 °С (рацемическая смесь оптических изомеров кислоты) |
| Разлагается при температуре 250°С | |
| Зольность | Менее 0,07% |
| Сахара | Менее 0,05% |
| Тяжелые металлы (свинец, медь, железо) | Менее 10 ppm |
| Мышьяк | Менее 0,2 ppm |
| Общий азот | Менее 250 ppm |
Уксусная кислота
Уксусная кислота (СН3СООН) была известна еще в древности как острый винный уксус (4-5%-ная уксусная кислота); концентрированная кислота была получена Шталем {Stahl) примерно в 1700 г. Соли уксусной кислоты содержатся в соках растений, в молоке, а также в некоторых выделениях животных — например в поте. Ацетаты являются конечным продуктом многих видов аэробного брожения.
В чистом виде это вещество — сильная агрессивная кислота, жидкость с характерным едким запахом.
Уксусную кислоту можно считать естественным слабым консервантом, и в этих целях она применяется в кондитерской промышленности при производстве марципана, миндальной пасты, а также некоторых видов помадных масс.
Состав:
| Удельная масса (15 °С/15 °С) | 1,055 |
| Температура кипения | 118 °С |
| Температура плавления | 17 °С |
Предотвращение брожения. Уксусная кислота
Далее рассматривается связь между составом ореховых паст, наличием микроорганизмов и сроком годности изделий. Пасты, используемые в качестве основы и произведенные с использованием только сахарного сиропа, обладают недостаточным содержанием растворимых сухих веществ, что не позволяет предотвратить брожение. В то же время в некоторых орехах содержатся осмофильные организмы, которые могут быть активны и в сиропах более высокой концентрации.
Брожения в таких пастах можно избежать при соблюдении следующих требований:
- проведение надлежащей мойки и дезинфекции оборудования;
- поддержание концентрации сиропной фазы на уровне выше 75%;
- стерилизация ореховой массы.
Были проведены исследования возможности использования уксусной кислоты в качестве консерванта в тех случаях, когда из соображений определенных требований к текстуре изделий или из-за особенностей применяемой технологии не удается выполнить все перечисленные выше требования. Эксперименты, проведенные с использованием помадных масс, концентрация сиропной фазы в которых составляла 70-75%, показали, что добавление 0,05-0,07% уксусной кислоты позволяет предотвратить брожение после инокуляции помадной массы дрожжами. Для марципановой пасты требуется большее количество кислоты (до 0,15%). Когда содержание кислоты превышает 0,10%, ее вкус заметен почти всем, а некоторые ощущают и присутствие значительно меньшего количесства кислоты (неприятный вкус иногда замечается даже при концентрации 0,05%).
Уксусная кислота должна обязательно распределяться в сиропе равномерно. В настоящее время шире применяют более эффективную сорбиновую кислоту (см. ниже).
Сорбиновая кислота
Сорбиновая кислота (СН3—СН=СН—СН=СН—СООН) является органиче- ской кислотой; ее стали широко использовать из-за присущих ей антибактериальных свойств. В природе она встречается в соке несозревшей ягоды рябины (ЗогЬш аисирапа, рябина обыкновенная) и в чистом виде представляет собой белый кристаллический порошок с приятным слегка кисловатым вкусом. Температура плавления — 130-134 °С.
В настоящее время эта кислота признана в качестве безвредного консерванта (издавна известны консервирующие свойства рябины, которую используют при приготовлении фруктовых пресервов для предотвращения плесени).
Сорбиновая кислота наиболее эффективно действует в кислой среде — pH должен быть менее 6. В таких условиях кислота подавляет активность плесневых и дрожжевых грибов, а также некоторых бактерий.
При условии соблюдения вышеуказанных требований к концентрации и стерильности для большинства видов кондитерских изделий консервирование не требуется, но для некоторых видов ореховой пасты, мягких начинок и фруктового пюре консервирование с помощью сорбиновой кислоты может оказаться полезным.
Нормы. В разных странах требования к применению сорбиновой кислоты различны, в связи с чем следует обращаться к действующим нормативным документам. Примерное представление об использовании этой кислоты в пищевых продуктах дают следующие цифры:
| Джемы, консервы (pH около 3,5) | 0,025%; |
| Фруктовые сиропы, ликеры | 0,02%; |
| Помадные массы, марципан, кондитерские пасты | 0,10-0,20%. |
Хотя более предпочтительно добавлять сорбиновую кислоту в горячий сироп или уже в кондитерские массы, можно приготовить и ее исходный раствор, представляющий собой раствор карбоната натрия в отношении 1 часть сорбиновой кислоты к 1,25 частям карбоната натрия. После добавления кислоты сироп не следует кипятить. Растворимость сорбиновой кислоты приведена в табл. 16.1.
Таблица 16.1. Растворимость сорбиновой кислоты
| Растворитель | Температура, С | Растворимость, % |
| Вода | 20 | 0,16 |
| 50 | 0,6 | |
| Этиловый спирт (95%-ный) | 20 | 14,0 |
| Глицерин | 20С | 0,5 |
Ортофосфорная (фосфорная) кислота
Ортофосфорная или просто фосфорная, кислота (Н3Р04) может поставляться в чистом виде, подходящем для использования в пищевом производстве. Она выпускается в двух видах, отличающихся по концентрации:
90%-ная Н3Р04 — удельная масса 1,75;
67%-ная Н3Р04 — удельная масса 1,50.
Эту кислоту иногда используют в качестве подкислителя пищевых продуктов, особенно безалкогольных напитков. Кроме того, ее применяют в качестве частично нейтрализующей кислоты для какао после обработки щелочами, но в некоторых странах ее использование запрещено (в этих целях чаще используют винную или лимонную кислоты). Фосфорная кислота и фосфаты применяются в пищевой промышленности в качестве ингредиентов моющих средств.
Состав:
| Удельная масса 1,75 | Удельная масса 1,5 | |
| Температура кипения | 171 °С | 123 °С |
| Температура замерзания | 28 °С* | -58 °С |
| Мышьяк** | Не более 2 ppm | |
| Свинец** | Не более 10 ppm |
* Фосфорная кислота с удельной массой 1,75 кристаллизуется при температуре окружающей среды.
** В соответствии с тестом фармакопеи Великобритании для пищевых ингредиентов.
Буферные и другие неорганические соли
В пищевые продукты, в том числе в шоколад, какао и кондитерские изделия, добавляют различные неорганические соли, допущенные к применению соответствующими нормативными актами. При использовании любых веществ такого рода необходимо, чтобы каждый контейнер поставщика был снабжен маркировкой с указанием названия вещества (или, по договоренности между поставщиком и заказчиком, его кодового обозначения). Когда без проверки использовали вещества из упаковки, не снабженной маркировкой или с ошибочной маркировкой, имели место недопустимые, опасные ошибки.
Даже в случае, когда кажется, что маркировка соответствует содержимому упаковок, специалист по контролю качества все равно должен периодически проверять соответствие веществ указанным наименованиям и чистоту их состава (хотя поставщик и предоставляет гарантии, а на маркировке указывается состав). Иногда в поставляемых веществах присутствуют мышьяк, свинец или другие тяжелые металлы, а бывает, что в упаковке с обозначением «пищевого сорта» оказывается технический сорт. Ниже мы приводим пределы допустимого содержания примесей, но рекомендуем всякий раз сверяться с соответствующими нормативами.
Цитрат натрия
Цитрат натрия ( С6Н507Nа3-2Н2О) представляет собой белый кристаллический порошок с солоноватым вкусом. При контакте с влажным воздухом он проявляет слегка гигроскопичные свойства, а в сухой среде теряет кристаллизационную воду, в связи с чем данное вещество должно храниться в герметично закрытых контейнерах.
Цитрат натрия используется в качестве буферной соли для контроля студнеоб- разования при производстве пектинового желе. В сочетании с антиоксидантами он характеризуется синергетическим действием, кроме того, утверждается, что он связывает медь и железо, играющие роль катализаторов прогорклости вследствие реакции окисления.
Моноцитрат натрия используется также в качестве буферной соли при кристаллизации, позволяя использовать сироп в ходе технологического процесса большее количество раз.
| Состав: | |
| Дигидрат | 99-101% |
| Кислотность/щелочность | Менее 0,5 мл 0,1 н NaOH/HCI в 2г |
| Хлориды | Не более 0,03% в пересчете на CI |
| Сульфаты | Не более 0,12% в пересчете на S04 |
| Тяжелые металлы (свинец, медь, железо) | Менее 10 ppm |
| Соль щавелевой кислоты | Отсутствует |
Молочнокислый натрий
Лактат натрия (СН3СН(ОН)СООNа) используется в качестве влагоудерживающего агента и пластификатора; промышленно используемый молочнокислый натрий представляет собой вязкий 70%-ный (% масс.) водный раствор. Активность воды у лактата в любых растворах ниже, чем у глицерина, и он с успехом применяется в качестве пластификатора пищевых продуктов на водной основе. Лактат может смешиваться с водой. Лактаты естественным образом присутствуют в пищевых продуктах и в организме человека; они не токсичны. При кипячении сахарный сироп используется вместе с молочной кислотой в качестве буферной соли.
Состав 70%-ного раствора:
| Удельная масса | 1,380 |
| pH, 10%-ное разведение | 7,0 |
| Показатель преломления | 1,435 |
| Температура замерзания | Ниже 10 °С |
| Равновесная влажность | 38%, aw 0,38 |
| Допустимые примеси | Как и для молочной кислоты |
Пирофосфорнокислый натрий, нейтральный пирофосфорнокислый натрий, тетрапирофосфат натрия («Тетрон»)
Пирофосфорнокислый натрий (Na4Р207) представляет собой белый порошок и является комплексообразующей солью; он обладает слабо выраженными щелочными свойствами. Это вещество применяется при производстве низкометоксилиро- ванного пектинового желе, поскольку связывает кальций, образующий при взаимодействии с этим типом пектинов гель. В этих целях на одну часть кальция требуется около четырех частей фосфата.
Состав:
| Растворимость при 20 °С | 5% |
| pH, 10%-ный раствор | 10,4 |
| Содержание Р205 | 53,5 % |
| Чистота в пересчете на 504 | Не более 0,25% |
| Хлор | Не более 0,2% |
| Мышьяк | Менее 1 ppm |
| Свинец | Менее 2 ppm |
| Железо | 25 ppm |
Битартрат калия (кислый виннокислый калий)
Кислый виннокислый калий (С4Н506К) выпадает в винном осадке и очищается затем с помощью рекристаллизации. В промышленности используется белый порошок, кислый на вкус. Это вещество применяется с целью вызвать процесс инвертирования при производстве изделий на основе сахарного сиропа, но в большинстве случаев вместо этого начали использовать контролируемое добавление инвертного сахара и глюкозы.
Инвертирование под действием кислого виннокислого калия будет ненадежным, если не обеспечить точного соблюдения продолжительности кипячения и строгого контроля щелочных свойств воды.
Состав:
| Растворимость при 20 °С 1 часть на 180 частей воды | |
| при 100 °С 1 часть на 15 частей воды | |
| Чистота | Аналогично винной кислоте |
Карбонат натрия (безводный), кальцинированная сода
Карбонат натрия (Nа2С03) применяется в основном для подщелачивания жидкой или порошковой заготовки при производстве какао. Иногда он применяется для нейтрализации кислых пищевых продуктов, но в этом случае чаще используется бикарбонат натрия.
Состав:
| Содержание Na2C03 Не менее 98,0% Мышьяк Не более 2 ppm Свинец Не более 5 ppm |
Кальцинированная сода при транспортировке и хранении может впитывать до 2% влаги, если у мешков, в которые она упакована, нет защитного внутреннего слоя.
Примеси мышьяка в кальцинированной соде стали предметом знаменитого дела «О мышьяке в какао», рассматривавшегося в английском суде в 1921 г. Несмотря на то что наличие этой примеси в настоящее время крайне маловероятно, необходимо все же не терять бдительности.
Двууглекислый натрий (пищевая сода)
Двууглекислый натрий (NаНС03) используется для нейтрализации кислых сиропов при вторичном использовании сырья (см. соответствующий раздел в главе 19). Это химическое вещество используется также для разрыхления и подъема изделий, так как при высоких температурах и примении кислотных компонентов выделяется углекислый газ:

Определяющую роль в обеспечении разрыхления готового кондитерского изделия играет распределение частиц по размерам. Этот вопрос рассматривается в разделе «Пористые кондитерские изделия» в главе 19.
Свойства пористых карамельных изделий будут значительно отличаться в зависимости от использования кислоты. Расщепление под действием только тепла приводит к повышению pH и к щелочной деструкции сахаров, в особенности декстрозы и фруктозы. Это придает изделиям типичный карамелизованный вкус и цвет. При расщеплении под действием кислоты pH остается на более низком уровне, благодаря чему получаются значительно более светлые изделия со слабо выраженным карамельным привкусом. Такой аэрированной карамели легче придать тонкий фруктовый вкус.
Бикарбонат натрия в сиропных суспензиях медленно расщепляется, и в случае их использования следует применять свежеприготовленные сиропы.
Состав:
| Бикарбонат натрия 99,0-101,0% в пересчете на NaHC03 Растворимость при 20 °С 1 часть на 11 частей воды Щелочные свойства (1%-ный раствор) pH не более 8,6 Мышьяк Не более 2 ppm Свинец Не более 5 ppm |
Другие химические вещества
В качестве вкусового вещества часто используют хлорид натрия (поваренную соль). Он обладает синергетическим эффектом по отношению к другим ароматам, и его часто добавляют в молочные конфеты и фадж. В какао-порошок для приготовления напитков добавляют от 0,5 до 1% соли.
Углекислый калий, гидроксид калия и гидроксид кальция используют в качестве подщелачивающих веществ для жидкого какао. Гидроксид кальция часто применяют в сиропах и молочных продуктах в качестве нейтрализатора.
Антиоксиданты
Об антиоксидантах мы уже упоминали в той части книги, где обсуждались микробиологические проблемы и прогорклость. Антиоксидатами называют натуральные или синтетические вещества, позволяющие задержать появление прогорклости вследствие реакции окисления.
Хотя исследования, посвященные антиоксидантам и механизмам их действия, начали проводиться сравнительно недавно, человек еще в доисторические времена использовал такие противоокислительные приемы, как копчение.
Давно известно, что консервирующим действием обладают некоторые травы, специи, а также овсяная мука; относительно недавно было обнаружено, что животные жиры прогоркают медленнее, если их смешивать с растительными.
Механизм возникновения прогорклости вследствие окислительных процессов
В первую очередь происходит самоокисление, начинающееся при контакте жира с воздухом. Активированные каким-либо внешним фактором (например светом, теплом или небольшим количеством примесей металлов), в жире образуются пероксидные радикалы, позволяющие вступать в реакцию с кислородом самому жиру. Так начинается непрерывная реакция. Порча жира измеряется при помощи определения пероксидного числа, и принято считать, что в животном жире прогорклость становится заметна на вкус при достижении пероксидным числом показателя 20, а в растительном масле — 50.
Время, необходимое для достижения пероксидным числом жира таких показателей, называется периодом индукции. Существует метод, позволяющий его измерять в искусственных условиях ускоренно — это так называемый тест Свифта (Swift test). При этом пузырьки воздуха пропускаются через определенное количество жидкого жира при температуре 98 °С. Пероксидное число измеряется через равные промежутки времени и отмечается на графике, а через некоторое время пероксидное число достигает 20 и на основе полученного графика определяется число Свифта. Существует несколько вариантов проведения этого теста.
Действие антиоксидантов и ограничения их применения
При замедлении образования пероксидов процесс прогоркания жира замедляется. Именно так и действуют антиоксиданты — как правило, это фенольные веще- ства, препятствующие механизму самоокисления, которые останавливают или замедляют описанную выше цепную реакцию.
В большинстве жиров животного и растительного происхождения содержатся естественные антиоксиданты, наиболее важными из которых являются токоферол (витамин Е) и лецитины. Их количество в зависимости от вида жира различно, и глицеридная структура некоторых жиров приводит к тому, что они более подвержены прогорканию. В растительных жирах обычно содержится больше естественных антиоксидантов, чем в животных, и из-за этого добавление антиоксидантов в животные жиры обеспечивает более заметный защитный эффект. Какао-масло, например, содержит такое большое количество естественных антиоксидантов и обладает настолько стабильной глицеридной структурой, что может очень долго сохранять свои свойства, не прогоркнув; при этом не требуется использование дополнительных антиоксидантов. Рыбий жир же, напротив, легко может прогоркнуть очень быстро, а добавление антиоксидантов обеспечит максимальное защитное действие. Естественные антиоксиданты имеют только частичный эффект, а в некоторых случаях они оказываются нетермостойкими — например при дезодорировании жира или глубоком прожаривании. Токоферолы и сами подвержены окислению и могут приводить к возникновению «рыбного» привкуса. Следует подчеркнуть, что антиоксиданты не могут служить в качестве защиты от прогорклости, вызванной реакцией гидролиза, появление которой можно определить по наличию «мыльного» привкуса и по увеличению кислотного числа, вызванному гидролизом жиров на глицерин и жирные кислоты. Прогорклость, вызванная окислением, придает продуктам салистый или рыбный привкус, а выявить ее аналитически можно на основе пероксидного числа.
Антиоксиданты не позволяют предотвратить изменение вкуса, которое иногда происходит в рафинированных жирах из-за химических изменений, происходящих еще до того, как начнется окисление. Наиболее эффективно действуют они тогда, когда их добавляют в свежие жиры, а когда жир уже начал портиться (например когда пероксидное число составляет уже от 10 до 20), пользы от введения антиоксидантов мало. Таким образом, пероксидное число является важным средств контроля партий жира, хранившихся в течение неизвестного времени. Но и в тех случаях, когда антиоксиданты добавляются в свежий жир, они не могут обеспечить его бесконечного хранения, и через какое-то время возможности антиоксиданта исчерпываются.
Реагенты-стабилизаторы (комплексообразователи), их синергическое действие. Некоторые вещества могут снижать каталитическое действие таких металлов, как медь и железо, которые, как известно, ускоряют развитие прогорклости, вызванной окислительными процессами. Эти вещества называются реагентами- стабилизаторами; состоят они из лимонной кислоты (а также некоторых цитратов), фосфорной кислоты и ЕВТА (этилендиаминатетрауксусной кислоты). Между первичными антиоксидантами наблюдается синергический эффект и, следовательно, наибольшую степень защиты обеспечивает сочетание комплекса антиоксидантов и реагента-стабилизатора.
Антиоксиданты, разрешенные к применению
В разных странах нормативные акты отличаются, и время от времени в них вносятся изменения. В справочниках и учебниках не следует приводить конкретные цифры, касающиеся таких ограничений, поскольку технолог пищевого производства должен самостоятельно следить за этой информацией, обращаясь к свежим журналам, а также специальным изданиям и нормативным актам.
Когда еще только начинали исследовать проблему антиоксидантов, было обнаружено, что большинство из них относятся к фенольным веществам. Хотя было выявлено множество антиоксидантов, широкое применение получили лишь четыре из синтетических веществ такого типа, а именно: бутилгидрооксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), третичный бутилгидрохинон (ТВНQ) и пропилгаллат.
Помимо этого рассматривался и вопрос о возможности применения октилгал- лата и додецилгаллата в сочетании с этоксихином для сохранения яблок и груш.
Воздействие антиоксидантов схематически изображено на рис. 16.1, где на графике показано изменение пероксидного числа со временем (данные получены в ходе эксперимента, заключавшегося в нагревании жира в потоке воздуха).
Естественные антиоксиданты
Негативная реакция потребителя на добавки иногда вынуждает производителей избегать применения синтетических антиоксидантов. Антиоксиданты присутствуют во многих натуральных продуктах, и в качестве примера можно привести токоферол, лецитин и аскорбиновую кислоту.
 Рис. 16.1. Влияние антиоксиданта на стабильность жира. По материалам фирмы N. V. Chemische
Рис. 16.1. Влияние антиоксиданта на стабильность жира. По материалам фирмы N. V. Chemische Fabriek, г. Наарден, Нидерланды
Химические формулы и свойства наиболее важных антиоксидантов приводятся в табл. 16.2.
Способы введения антиоксидантов
В растворе. Поскольку вводится очень небольшое количество, то антиоксидант можно легко растворить в некотором количестве жира или другого вещества, которое затем добавляется в общую массу.
Напылением или погружением. В случаях, когда требуется защитить продукты, обжариваемые в масле, раствор антиоксиданта может быть напылен на продукт либо антиоксидант растворяют в масле, которое часто применяют на последней стадии обжаривания орехов.
Упаковочные материалы и инструменты
Антиоксиданты добавляют и в упаковочные материалы, предназначенные для упаковки жиросодержащих пищевых продуктов, если есть вероятность, что жир проступит сквозь упаковку или тонким слоем распространится по ее поверхности. Тонкий слой жира очень подвержен прогорклости, вызванной реакцией окисления. Такое использование антиоксидантов вполне допустимо при условии, что в случае их переноса с упаковки на пищевой продукт не будет превышено их допустимое содержание в продукте.
Иногда окисляется слой упаковочного материала или покрывающий его лак, в результате чего вырабатывается ядовитое вещество. Для предотвращения этого также служат антиоксиданты.
В некоторых пластиках, из которых изготовлены инструменты и контейнеры для пищевых продуктов, могут содержаться антиоксиданты, не допущенные к использованию в контакте с пищевыми продуктами. Использование таких пластмассовых контейнеров для хранения продуктов может привести к выделению антиоксидантов, не разрешенных для контакта с пищевыми продуктами.
Смазки для форм, эмульгаторы
В процессе производства кондитерские изделия касаются формы, металлических деталей, конвейерной ленты из текстильного материала, боковых направляющих, а также разного рода инструментов. Кондитерские изделия в эти моменты часто бывают горячими, особенно леденцовая карамель. Когда горячий расплав выливается на металлический (или мраморный) стол, на ленту конвейера или в форму, если между кондитерским изделием и поверхностью не будет помещено какое-то вещество, оно может прилипнуть.
Такое вещество должно легко распределяться по поверхности, образовывать сплошную пленку, не смешиваться с продуктом и оставаться подвижным после

Примечание
Легко растворяется в жире. Воскоподобное твердое вещество. Эффективен для животного жира, менее эффективен для растительного. Не расщепляется при переработке пищевых продуктов. Состоит из двух изомеров. В промышленности применяется 90%-ный 3-третичный бутил-4-гидроксианизол, так как он действует наиболее эффективно
Сходен с ВНА, в сочетании с ним проявляется синергический эффект
Наиболее эффективный антиоксидант как для животных, так и для растительных жиров. Жирорастворим
охлаждения изделия. Кроме того, оно должно быть съедобным, без вкуса и запаха и обладать длительным сроком годности.
Простейшие смазки для форм — это сливочное масло, растительный жир или масло для смазки противней или форм для выпечки. В кондитерской промышленности первоначально применялись те же жиры, но от их использования пришлось отказаться из-за роста объемов производства и необходимости обеспечить увеличение срока хранения изделий, так как сливочное масло стоит дорого, а тонкий его слой, остававшийся на поверхности кондитерских изделий, быстро прогоркает. Хотя растительные масла используются иногда до сих пор, выбирать их следует очень тщательно, поскольку при хранении многие из них могут привести к появлению нежелательного запаха и привкуса.
В случае крупного непрерывного производства приходится смазывать конвейерные ленты и формы для кондитерских изделий. Важно обеспечить, чтобы любое вещество, которое используется в качестве смазки, обязательно сохраняло свои свойства в течение продолжительного времени, поскольку, несмотря на смазку форм в начале каждого цикла новой смазкой, некоторое количество первоначально нанесенной смазки все же остается.
В качестве альтернативы растительного масла достаточно широко используется специальное очищенное легкое минеральное масло для смазки форм — оно не имеет вкуса и запаха, химически неактивно и не прогоркнет. Минеральное масло допускается к такому использованию не везде, а там, где оно применяется, количество его остатка в составе употребляемого в пищу продукта регулируется нормативными документами.
Некоторые смазки для форм включаются в состав самого продукта — например это делается при производстве таблетированых изделий, поскольку здесь важна легкость их отделения от формы.
Типы смазок для форм
СПЕЦИАЛЬНЫЕ СМАЗКИ ДЛЯ ФОРМ, МИНЕРАЛЬНЫЕ МАСЛА
Эти масла, обладающие низкой вязкостью, очищены до такой степени, что вкус и запах у них отсутствуют и не появляются даже при расщеплении масла при высокотемпературной обработке леденцовой карамели.
Состав:
| Удельная масса 15,5 °С/15,5°С | 0,856-0,870 |
| Поведение при облучении ультрафиолетом | Едва заметное свечение |
| Карбонизируемые вещества | Следы (по тесту фармакопеи Великобритании) |
| Вкус | Отсутствует, нет характерного вкуса нефтепро дуктов |
Такие масла на смазанной поверхности держатся недолго, и масляную пленку приходится обновлять достаточно часто. За счет добавления кукурузного крахмала,
благодаря чему образуется паста, пленка смазки держится лучше и в некоторых рецептурах это используется весьма успешно, однако на готовых изделиях оказывается некоторое количество крахмала.
Ацетилированные моноглицериды
Эти вещества представлены на рынке под различными фирменными названиями и представляют собой моноглицериды, гидроксильная группа которых этерифи- цирована уксусной кислотой, после чего полученное вещество прошло дистилляцию. Считается, что благодаря присутствию полярных групп возникает ориентация молекул, обеспечивающая образование тонкой сплошной пленки, способной приклеиваться к разного рода поверхностям. Эти вещества можно представить в виде следующей формулы:

Эти вещества также могут использоваться в качестве защитной глазури, препятствующей высыханию изделий, а также развитию прогорклости (см. раздел «Арахис», глава 15). Некоторые из этих соединений наносят на поверхность драже, придавая ему блеск.
В прошлом при использовании этих соединений возникали некоторые проблемы, поскольку при хранении изделий такое покрытие начинало придавать им нежелательный запах, но производители гарантируют, что в настоящее время поставляемые ими вещества лишены этого недостатка.
Тончайший слой, присутствующий на поверхности изделий, на которую нанесли покрытие, контактирует с воздухом и из-за этого подвержен окислению, в связи с чем для покрытия следует подбирать устойчивые к окислению компоненты.
Воскообразные смазки для форм
Такой тип смазки состоит из эфиров длинноцепочечных жирных кислот и высокомолекулярных спиртов с одной гидроксильной группой. Достаточно известным среди продуктов такого типа является Воезоп Тгепптах, поставляемый в твердой и жидкой формах, а также в виде аэрозоля.
Это безводное вещество устойчиво к действию высоких температур, которым оно подвергается при выпечке или при производстве леденцовой карамели. Жалоб по поводу возникновения в результате его использования нежелательного привкуса не поступало.
Смазки для форм из лецитина и жира
Смеси лецитина и жира представляют собой смесь синтетического лецитина (УА) и какао-масла; они вполне успешно применяются для смазки форм. Первый раз наносится состав, состоящий из смеси УЗУ и какао-масла (50/50). В дальнейшем для смазки применяется только какао-масло. Для отделения изделий от формы температура должна быть не ниже 38 °С. Нанесение одного только какао-масла обеспечивает отделяемость от формы в течение не менее двенадцати циклов, после чего необходимо обновить пленку из содержащей лецитин смеси.
Силиконовые соединения
Очень подходит для применения в кондитерской промышленности силиконовый каучук, обладающий отличными противопригарными свойствами и выдерживающий воздействие высоких температур.
Этот материал используется для производства форм для отливки молочных конфет и подобных им кондитерских изделий, извлечение которых облегчается гибкостью форм. Это вещество все еще обходится достаточно дорого, но затраты компенсируются преимуществами, возникающими благодаря возможности механизации производства.
Силиконовые покрытия и смазки наносятся на конвейерные ленты, секачи и противни для выпечки. Иногда их наносят на внутреннюю поверхность котлов при концентрировании таких чувствительных продуктов, как фруктовое пюре. Следует отметить, тем не менее, что такое покрытие при контакте со слегка царапающимися кондитерскими изделиями (например фаджем или помадкой) легко нарушить.
Тефлон (политетрафторэтилен, ПТФЭ)
Это вещество обладает чрезвычайно низким коэффициентом трения и хорошо известно в качестве внутреннего покрытия домашней утвари. В кондитерской промышленности тефлоновое покрытие наносят на секачи для липких паст и молочных конфет, а также на раскатывающие вальцы. Из этого материала изготавливают также боковые направляющие конвейера.
На упаковочных машинах тефлоновую ленту применяют в качестве промежуточного слоя, предотвращающего прилипание к упаковочным материалам горячих запаивающих кромок.
Прочие вещества, используемые в качестве смазки для форм
Сюда входят такие вещества, как стеариновая кислота и стеарат магния.
Спермацетовый воск, карбонат кальция, а также многие другие вещества в специальной литературе называют в числе «смазок для форм» или их компонентов.
Производителями эмульгаторов и других подобных веществ выпускаются брошюры, в которых подробно рассматриваются их свойства и применение.
Эмульгаторы
Для производства покрытий из шоколада и смесей используются лецитин, сор- битан (сложные жирные эфиры) и полирицинолеат полиглицерина. Лецитин также используется для производства кондитерских изделий. Еще одним важным эмульгатором является глицерилмоностеарат (6М5). Глицерилмоностеарат напоминает жир, представляя собой сочетание жирной кислоты с глицерином, но отличается от жира тем, что связана только одна из его ОН-групп:

Промышленные моностеараты состоят не только из моностеаратов, представляя собой смесь моно-, ди- и тристеаратов, но активным эмульгатором является все же моностеарат. Они выпускаются и в самоэмульгирующейся форме — в этом случае в состав включено 3-6% стеарата натрия, благодаря чему для эмульгирования этого вещества достаточно энергично его размешать в горячей воде с температурой 88-90 °С.
Технические характеристики наиболее распространенных продуктов на основе глицерилмоностеарата приведены в табл. 16.3.
Таблица 16.3. Характеристики продуктов на основе глицерилмоностеарата
| СМ8 35 | СМБбб | вМБ Э/Р | |
| Свободные жирные кислоты (на олеиновую кислоту), % | Не более 0,4 | Не более 0,4 | Не более 0,4 |
| «Мыла», % | 2,7-3,3 | 5,5-6,5 | Не более 0,3 |
| Влага, % | Не более 2,0 | Не более 2.0 | Не более 2,0 |
| Моноглицерид, % | Не менее 32,5 | Не менее 32,5 | Не менее 32,5 |
| Свободный глицерин, % | Не более 5 | 4-6 | Не более 5 |
| Температура плавления, °С | 56-60 | 56-60 | 56-60 |
| Число омыления | 177-183 | 177-183 | 177-183 |
В производстве молочных конфет и фаджа глицерилмоностеарат выполняет важную функцию — он существенно способствует эмульгированию входящего в состав жира. При их экструзии для производства плиток моностеарат предотвращает отделение жира. В составе конфетной массы из тертого ореха (например той, которая используется в батончиках с кокосом) благодаря добавлению моностеарата происходит эмульгирование всего масла, выделяющегося из ореховой массы при ее переработке.
В составе начинок (например, творожной массы с лимоном) моностеарат используется для предотвращения отделения жира при последующем нагревании. Его эмульгирующая способность особенно важна в производстве выпечки и мороженого.
Растворители
Для растворения ароматизаторов и других веществ в кондитерской промышленности используются разные виды растворителей. Ингредиенты в виде раствора равномерно распределяются по всему изделию.
Растворители входят в состав комбинированных ароматизаторов и концентратов «добавок». Практически во всех областях применяются четыре из существующих растворителей — этиловый спирт, глицерин, пропиленгликоль и изопропиловый спирт.
Из растворителей разных областей применения можно выделить:
- моноацетат глицерина (моноацетин);
- диацетат глицерина (диацетин);
- триацетилглицерин (триацетин);
- диэтиловый эфир и этилацетат.
Относительно применения растворителей, как и в случае с пищевыми добавками, необходимо руководствоваться нормативными актами, действующим в каждой отдельной стране. В некоторых странах использование растворителя может допускаться только в определенных дозировках или только для определенных веществ.
К выбору растворителей следует подходить очень тщательно, так как даже соблюдая принятые во многих странах требования по использованию растворителей в пищевых продуктах, можно столкнуться с различиями их по чистоте. Важно проверить наличие в составе растворителей таких веществ, которые, присутствуя даже в ничтожных количествах, могут придавать пищевым продуктам нежелательный привкус.
Этиловый спирт, этанол
Этиловый спирт (С2Н5ОН) используется обычно в форме ректифицированного спирта, который на 95% об. состоит из этилового спирта. Это высокоочищенный спирт, не имеющий постороннего вкуса или запаха. Из-за того, что он облагается акцизной пошлиной, этот растворитель стоит достаточно дорого.
Состав:
| Содержание спирта | 94,7-95,2% об. |
| 92,0-92,7% масс. | |
| Удельная масса (при 20 °С) | 0,8119-0,8139 |
| Показатель преломления (20 °С) | 1,3637-1,3639 |
| Нелетучий остаток (при 105 °С) | Не более 0,005% масс./об. |
Глицерин
Глицерин (СH2ОНСНОНСН2ОН) поставляется в нескольких видах — в сыром, слабой очистки и химически чистом виде, но в качестве растворителя следует использовать только последний из них.
Ароматизаторы, красители и некоторые другие ингредиенты ограниченно растворимы в глицерине. Для повышения их растворимости глицерин иногда разбавляют водой. Перед использованием глицерина всегда необходимо провести испытания, обращая особое внимание на перенасыщение, так как из-за него при хранении изделий может выпадать твердый осадок. Глицерин способен смешиваться с водой и спиртом. В некоторых рецептурах кондитерских изделий глицерин используется в качестве влагоудерживающего агента и «умягчителя» — обычно его количество составляет 2-3%. Его применяют также в кондитерских изделиях, хранящихся в замороженном виде, так как глицерин позволяет им оставаться мягкими и при низких температурах.
Состав:
| Удельная масса (при 20 °С) | 1,255-1,260 |
| Показатель преломления (20 °С) По тестам фармакопеи Великобритании: | 1,471-1,474 |
| Наличие примесей: | Свинец — менее 1 ppm Мышьяк — менее 2 ppm |
| Медь | Смешать 10 мл глицерина с 30 мл воды, 1 мл соляной кислоты и 10 мл раствора сероводорода; полученный состав не должен окрашиваться. |
| Редуцирующие вещества | Смешать 5 мл глицерина с 5 мл разбавленного раствора аммиака и нагреть до 60 °С , поддерживая эту температуру в течение 5 мин. Быстро добавить 0,5 мл раствора нитрата серебра, который следует капать пипеткой, кончик которой располагается выше горлышка пробирки так, чтобы реагент капал прямо в раствор, а не на стенки пробирки. Перемешать и оставить в темном месте на 5 мин; состав не должен потемнеть. |
| Кислотные/щелочные свойства | 10%-ный (масс./об.) раствор нейтрален по отношению к лакмусовому раствору. |
Пропиленгликоль, 1,2-пропандиол
Пропиленгликоль (СН8СНОНСН2ОН) представляет собой вязкую жидкость без цвета и запаха, напоминающую глицерин, со слегка сладким вкусом. Он смешивается с водой и спиртом, гигроскопичен. Используется для растворения многих пищевых красителей, эфирных масел, ароматизаторов и олеосмол; постепенно пропиленгликоль становится основным растворителем в кондитерской промышленности.
Состав:
| Удельная масса при 15 °С/15 °С | 1,0409 |
| То же при 20 °С/20 °С | 1,0381 |
| Показатель преломления (20 °С) | 1,4326 |
| Температура кипения | 187 °С (95 % дистиллируется в диапазоне температур 187-189 °С) |
| Температура воспламенения | 107 °С |
| Кислотность (в пересчете на уксусную кислоту), % | Не более 0,005 |
| Зольность, % | 0,005 |
| Влага, % | Не более 0,2 (Внимание! Пропиленгликоль гигроскопичен) |
| Температура замерзания (для 60%-ного раствора) | -60 °С |
Изопропиловый спирт, пропанол-2
Изопропиловый спирт (СН3СН(ОН)СН3) представляет собой бесцветную жидкость с характерным запахом, кипящую при низкой температуре. Он должен состоять как минимум из 99,5% масс, чистого изопропилового спирта. Хотя чаще всего при использовании небольших количеств этого растворителя при производстве кондитерских изделий его вкус и запах не ощущаются, некоторые люди его замечают и находят неприятным.
Когда этот разбавитель только начали использовать в пищевой промышленности, случалось, что при дистилляции некоторые его виды давали сильный привкус, но в настоящее время используются чистые пищевые сорта и таких проблем уже не возникает.
Состав:
| Удельная масса при 20 °С/20 °С | 0,785-0,787 |
| Показатель преломления (20 °С) | 1,378 |
| Температура кипения | 82 °С диапазон — 81,5-83 °С |
| Остаток при дистилляции | Не более 2 мг на 100 мл (не должен иметь |
| ни запаха, ни вкуса) | |
| Кислотность по уксусной кислоте, % | Не более 0,002 |
| Температура замерзания | -89,5 °С |
Концентрат инвертазы
Инвертаза — очень активный ферментный препарат, экстрагируемый из дрожжевых культур. Он приводит к гидролизу сахарозы в инвертный сахар. Промышленное применение находит жидкий концентрат инвертазы под различными фирменными названиями.
Существуют два фермента, обеспечивающих гидролиз сахарозы: β-h-фруктозидаза и α-n-глюкозидоинвертаза. Первый из них воздействует на фруктозную, а второй — на глюкозную часть молекулы сахарозы. Промышленная инвертаза изготавливается из дрожжей и содержит β-h-фруктозидазу, оптимальными условиями для действия которой является pH 4-5. α-n– глюкозидоинвертазу получают из гриба Aspergillus oryzae, а α-глюкозидазу — из сухих дрожжей; она приводит к гидролизу сахарозы при pH 6-7.
Для получения инвертазы используется особый штамм дрожжей, который выращивается в условиях, стимулирующих повышенное ее выделение. При промышленном производстве эту культуру размножают путем глубокого аэробного брожения. Затем полученные дрожжи доводятся до нужной кондиции с помощью обработки мелассой при аэрировании, в результате чего становится возможен лишь незначительный их рост, но выделение инвертазы возрастает в два или три раза. Экстрагирование фермента производится путем плазмолиза, после чего следует автолиз, то есть сбраживание под действием протеолитического фермента. Плазмолиз проводится при повышенной температуре путем добавления толуола, после чего усваивается папаин, а затем путем фильтрования удаляются оставшиеся клетки. Фильтрат охлаждается, pH доводится до 4,5 и фермент осаждается под действием охлажденного технического спирта, в результате чего получается вещество, называемое инвертазной смолой. При промышленном производстве инвертазы этот осадок чаще всего растворяют в 55%-ном глицерине, определяют уровень ее активности, после чего раствор доводят до стандартной концентрации. Помимо инвертазы в растворе в продаже имеются и ее сухие технические препараты. При производстве этого продукта сушка осуществляется в условиях, позволяющих полностью подавить жизнеспособность дрожжей, не снижая активности инвертазы.
Использование инвертазы в приготовлении помадной массы
В кондитерской промышленности инвертаза используется в основном для инвертирования сахарозы в конфетной начинке из помадной массы перед ее отсадкой в форму и покрытием шоколадом. Благодаря инвертированию текстура помадной массы становится более мягкой; кроме того, благодаря гигроскопичности фруктоз- ной (левулозной) составляющей инвертного сахара предотвращается засыхание изделий. Присутствие инвертного сахара изменяет состав массы, увеличивая долю содержания жидкой фазы, что позволяет снизить вероятность дальнейшей нежелательной кристаллизации и является дополнительным средством защиты против брожения. В случае применения этой технологии помадная масса приобретает такую текстуру, что массу невозможно было бы извлекать из крахмальных форм могуль-машины.
Производство помадной массы описано в главе 19; отметим, что она состоит из твердой фазы, представляющей собой мельчайшие кристаллы сахарозы, рассредоточенные в жидкой фазе, состоящей из использованного в конкретной рецептуре глюкозного сиропа и насыщенного раствора сахара.
Такую помадную массу можно вновь довести до жидкого состояния при температуре 60-65 °С — на этом этапе добавляются ароматизаторы, красители и другие ингредиенты, например повидло, фрукты или фраппе (яичный белок, взбитый с сиропом до пенообразного состояния), а также концентрат инвертазы. Затем эта масса отливается в ячейки лотков, заполненные кукурузным крахмалом, а затем остывшие и затвердевшие помадные корпуса освобождаются от крахмала и очищаются щеточным механизмом. Затем они глазируются, и через некоторое время помадная масса под действием инвертазы приобретает полужидкую консистенцию.
Как и в случаях с любыми другими ферментами, на активность инвертазы оказывают заметное влияние условия окружающей среды. При производстве помадной массы и сиропов важными факторами являются pH, температура и процентное содержание растворимых сухих веществ, а также постоянное количество инвертазы. Скорость действия может также зависеть от количества используемого концентрата инвертазы, которое, в соответствии с рекомендациями различных ее производителей, должно составлять от 28,3 до 87,9 г на 45,3 кг помадной массы. Степень инвертирования сахарозной составляющей в помадной массе связана с вышеописанными условиями. Если концентрация растворимых сухих веществ слишком высока, то активность значительно замедляется и сахароза инвертируется не полностью. Если помадные корпуса, извлеченные из крахмальных форм, имеют низкую влажность, то в дальнейшем может произойти незначительное изменение (разжижение) консистенции (см. далее).
Лучше всего инвертаза действует в слегка кислой среде (оптимальной является pH 4,5-5). Если pH будет выше этого уровня, то действие инвертазы будет происходить медленнее, а при превышении pH 7 оно прекращается. Как видно из рис. 16.2, при концентрации 50% и ниже оптимальная температура для действия инвертазы составляет 60 °С. Такие же условия создаются и при производстве инвертного сахара с использованием инвертазы, при этом также регулируется pH. В случае более высокого уровня содержания растворимых сухих веществ в помаде могут допускаться более высокие температуры, но при температурах выше 65,6 °С происходит значительное снижение активности инвертазы. Снижение активности инвертазы в усредненной помадке при различных температурах в течение 20 и 30 мин повторного разжижения приведено в табл. 16.4.
 Рис. 16.2. а — влияние концентрации на скорость инвертирования; Ь — влияние температуры на скорость инвертирования; с — влияние pH на скорость инвертирования. Содержание сиропа в концентрате инвертазы — 0,15 %; pH = 5,0 (а и б). Температура — 60 °С (а и с). По [12]
Рис. 16.2. а — влияние концентрации на скорость инвертирования; Ь — влияние температуры на скорость инвертирования; с — влияние pH на скорость инвертирования. Содержание сиропа в концентрате инвертазы — 0,15 %; pH = 5,0 (а и б). Температура — 60 °С (а и с). По [12] Таблица 16.4. Снижение активности инвертазы при различных температурах
| Снижение активности (%) в течение: | ||
| °С | 20 мин | 30 мин |
| 60,0 | 4 | 6 |
| 65,6 | 8 | 12 |
| 71,1 | 15 | 20 |
| 76,7 | 20 | 30 |
При температуре 82,2 °С и выше теряется как минимум 70% активности инвертазы. Следует отметить, что даже при обычных температурах темперирования (60-65,6 °С) происходит значительное снижение активности, если помадная масса отсаживается в формы через некоторое время. Ингредиенты, добавляемые в помадную массу (сахар, яичный альбумин, молочные продукты, дробленые орехи, желатин, агар-агар, жир и модифицированный крахмал), оказывают на активность инвертазы весьма незначительное влияние, но весьма пагубное воздействие при смешивании с неразбавленным концентратом инвертазы могут оказать ароматизаторы и красители. Особенно разрушительное действие могут оказывать растворы ароматизаторов, в связи с чем совершенно необходимо, чтобы добавление всех ингредиентов в помадную массу и доведение ее до температуры плавления осуществлялось еще до того, как будет добавлена инвертаза. В этом случае фермент до отсаживания массы в крахмальные формы успевает лишь равномерно распределиться в составе массы. В инвертазе могут содержаться тяжелые металлы, но в кондитерском производстве нежелательную примесь может создать только медь (в количестве 1-2 ppm). В промышленности все еще используется медная посуда, но единственная необходимая мера безопасности состоит в том, чтобы не допускать непосредственного контакта концентрата инвертазы с поверхностью медной посуды. Скорость инвертирования зависит от содержания влаги в помадке, а также от температуры хранения. При температуре около 18 °С, содержании влаги в 12,5-13,0% и содержании растворимых сухих веществ в сиропе 76% максимальное инвертирование происходит примерно через два месяца.
Если же по какой-либо причине помада утрачивает влагу (например в случае слишком позднего глазирования или пересыхания при хранении), то действие инвертазы прекратится при достижении 80%-ной концентрации растворимых СВ.
Производство инвертного сахара
Процесс производства инвертного сахара из отходов производства с использованием инвертазы описан в главе 8, но иногда требуется изменить температуру или концентрацию (см. рис. 16.2). Из соображений экономичности следует определить, потребуется ли использовать сироп высокой или низкой концентрации, — это будет зависеть от того, как будут растворять вторичное сырье, и от того, как оно будет использоваться после инвертирования. Также требуется тщательно оценивать количество используемой инвертазы, которое зависит от продолжительности процесса инвертирования.
Литература
АНТИОКСИДАНТЫ
- Antioxidants in Food Regulations. Her Majesty’s Stationary Office, London.
- Buck, D. F. Antioxidant applications. Manf. Conf. (June)> 1985.
- Eastman Chemical Products Inc., Kingsport, Term.
- Ostendorf, J. F. Naarden, Bussum, Holland.
СМАЗКИ ДЛЯ ФОРМ, ЭМУЛЬГАТОРЫ
Фирменные материалы:
- Boehringer GmbH, Ingelheim, W-Germany.
- Croda Food Products Ltd., Goole, England.
- Eastman Chemical Products Inc., Kingsport, Tenn.
- Grinsted Products A/S, Brabrand, Denmark.
- Imperial Chemical Industries Ltd., London.
Ф ЕРМЕНТЫ, ИНВЕРТАЗА
- Cochrane, A. L. Production and application of enzyme preparation in food manufacture. SCI Monograph No. 11 // Soc. Chem. Ind. — London, 1961.
- Dixon, М., Webb, E. C. Enzymes (2nd. ed.). — Harlow, England: Longman, 1964.
- Janssen, F. Manufac. Confect. — 1961. — N9 1. — P. 56 (Aug., U.S.A).
- Minifie, В. W., Carpenter, W. J. Micro-organisms in confectionery industry // Proc. Biochem. (May). — London, 1966.
- Novo Industri, A/S 1986. Bagsvaerd, Denmark.
ПРОЧЕЕ
- Directory of Equipment and Supplies. 1986. Manf. Conf. (July).
- Food Additives — The Professional and Scientific Approach. — Institute of Food Science and Technology. — London, 1986.
- Solvents: Egan, H., Kirk, R. S., Sawyer, R. Pearsons Chemical Analysis of Foods. — Edinburgh, Scotland: Churchill-Livingstone, 1981.
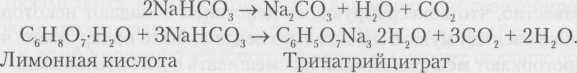
Останні коментарі